При входе на сайт вы даете согласие на обработку персональных данных в соответствии с пользовательским соглашением
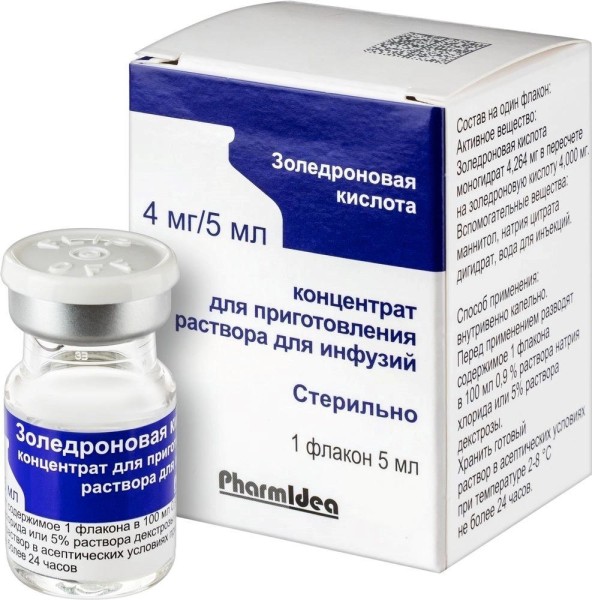
Внешний вид упаковки может отличаться от фотографии
Золедроновая кислота конц. д/р-ра д/инф. 4 мг/5 мл 5 мл №1
Мир-Фарм ООО, произведено ООО Фармидея, Россия
Регистрационный номер
ЛП-003688
Торговое название
Золедроновая кислота
Международное непатентованное название
Золедроновая кислота
Лекарственная форма
Концентрат для приготовления раствора для инфузий
Состав
на один флакон:
Активное вещество:
Золедроновая кислота моногидрат 4,264 мг
в пересчете на золедроновую кислоту 4,000 мг
Вспомогательные вещества:
Маннитол 220,000 мг
Натрия цитрата дигидрат 24,000 мг
Вода для инъекций до 5 мл
Прозрачная бесцветная или слегка желтоватая жидкость
Фармакотерапевтическая группа
Ингибитор костной резорбции, бисфосфонат
Код ATХ
М05ВА08
Фармакологические свойства
Фармакодинамика
Золедроновая кислота относится к высокоэффективным бисфосфонатам, избирательно действующим на кость. Препарат подавляет резорбцию костной ткани, воздействуя на остеокласты.
Селективное действие бисфосфонатов на костную ткань основано на высоком сродстве к минерализованной костной ткани. Точный молекулярный механизм, обеспечивающий ингибирование активности остеокластов, до сих пор остается невыясненным. Золедроновая кислота не оказывает нежелательного воздействия на формирование, минерализацию и механические свойства кости.
Помимо ингибирующего действия на резорбцию кости, золедроновая кислота обладает противоопухолевыми свойствами, обеспечивающими эффективность препарата при костных метастазах:
- In vivo: ингибирование остеокластической резорбции костной ткани, изменяющее микросреду костного мозга, приводящее к снижению роста опухолевых клеток; анти-ангиогенная активность. Подавление костной резорбции клинически сопровождается в том числе выраженным снижением болевых ощущений.
- In vitro: ингибирование пролиферации остеобластов, прямая цитостатическая и проапоптическая активность, синергичный цитостатический эффект с противоопухолевыми препаратами; антиадгезивная/инвазивная активность.
Золедроновая кислота, подавляя пролиферацию и индуцируя апоптоз, оказывает непосредственное противоопухолевое действие в отношении клеток миеломы человека и рака молочной железы, а также уменьшает проникновение клеток рака молочной железы человека через экстрацеллюлярный матрикс, что свидетельствует о наличии у неё антиметастатических свойств. Кроме того, золедроновая кислота ингибирует пролиферацию клеток эндотелия человека и у животных оказывает антиангиогенное действие.
У больных раком молочной железы, предстательной железы и другими солидными опухолями с метастатическим поражением костей золедроновая кислота предотвращает развитие патологических переломов, компрессии спинного мозга, снижает потребность в проведении лучевой терапии и оперативных вмешательств, уменьшает опухолевую гиперкальциемию. Препарат способен сдерживать прогрессирование болевого синдрома. Лечебный эффект менее выражен у пациентов с остеобластическими очагами, чем с остеолитическими.
У больных множественной миеломой и раком молочной железы при наличии как минимум одного костного очага эффективность золедроновой кислоты в дозе 4 мг сравнима с памидронатом в дозе 90 мг.
У больных с опухолевой гиперкальциемией действие золедроновой кислоты характеризуется снижением уровня кальция в сыворотке крови и выделения кальция почками. Среднее время до нормализации уровня кальция составляет около 4 дней. К 10-му дню концентрация кальция нормализуется у 87-88% больных. Среднее время до рецидива (скорректированный по альбумину уровень кальция сыворотки не менее 2,9 ммоль/л) составляет 30-40 дней. Значимых различий между эффективностью золедроновой кислоты в дозах 4 и 8 мг при лечении гиперкальциемии не наблюдается
Исследования не выявляют значимых различий в отношении частоты и тяжести нежелательных явлений, наблюдающихся у пациентов, получавших золедроновую кислоту в дозах 4 мг и 8 мг, памидронат в дозе 90 мг или плацебо как при лечении костных метастазов, так и гиперкальциемии.
Фармакокинетика
Фармакокинетические параметры не зависят от дозы препарата.
После начала инфузии золедроновой кислоты сывороточная концентрация быстро увеличивается, достигая пика в конце инфузии, далее следует быстрое уменьшение концентрации на 10% после 4 часов и на менее чем 1% пика после 24 часов с последовательно пролонгированным периодом низких концентраций, не превышающих 0,1% от максимальной, до повторной инфузии на 28 день.
Золедроновая кислота, введенная внутривенно, выводится почками в три этапа: быстрое двухфазное выведение препарата из системной циркуляции с периодами полувыведения 0,24 ч и 1,87 ч и длительная фаза с конечным периодом полувыведения, составляющим 146 ч. Не отмечено кумуляции препарата при повторных введениях каждые 28 дней. Золедроновая кислота не подвергается метаболизму и выводится почками в неизменном виде. В течение первых 24 часов в моче обнаруживается 39 ± 16 % введенной дозы. Остальное количество препарата в основном связывается с костной тканью. Затем медленно происходит обратное высвобождение золедроновой кислоты из костной ткани в системный кровоток и её выведение почками. Общий плазменный клиренс препарата составляет 5,04 ± 2,5 л/ч и не зависит от дозы препарата, пола, возраста, расовой принадлежности и массы тела пациента. Увеличение времени инфузии с 5 до 15 минут приводит к уменьшению концентрации золедроновой кислоты на 30 % в конце инфузии, но не влияет на площадь под кривой «концентрация-время» (AUC).
Фармакокинетические исследования у пациентов с гиперкальциемией или поражением функции печени не проводились. По данным, полученным in vitro, золедроновая кислота не ингибирует изоферменты системы цитохрома Р450 и не подвергается биотрансформации, что позволяет предположить, что состояние функции печени сколько-нибудь существенным образом не влияет на фармакокинетику золедроновой кислоты. Через кишечник выводится менее 3 % дозы препарата.
Почечный клиренс золедроновой кислоты положительно коррелирует с клиренсом креатина и составляет 75 ± 33 % от клиренса креатинина (КК), составляющего в среднем 84 ± 29 % (диапазон 22-143 мл/мин). У пациентов с клиренсом креатинина 20 мл/мин (тяжелая почечная недостаточность) или 50 мл/мин (умеренная почечная недостаточность) рассчитанный клиренс золедроновой кислоты составляет 37 % и 72 % соответственно, от значения клиренса золедроната у пациентов с клиренсом креатинина 84 мл/мин. Фармакокинетические данные у пациентов с тяжелой почечной недостаточностью (КК менее 30 мл/мин) ограничены.
Показано низкое сродство золедроновой кислоты к клеточным компонентам крови, связывание с белками плазмы низкое (около 56 %) и не зависит от концентрации золедроновой кислоты.
Показания к применению
• Метастазы в кости при злокачественных солидных опухолях (рак предстательной железы, рак молочной железы и другие) и множественная миелома, в том числе, для снижения риска патологических переломов, компрессии спинного мозга.
• Гиперкальциемия (концентрация скорректированного по альбумину сывороточного кальция ? 12 мг/дл или 3 ммоль/л), обусловленная злокачественными опухолями.
Противопоказания
• Повышенная чувствительность к золедроновой кислоте, другим бисфосфонатам или любым другим компонентам, входящим в состав препарата.
• Нарушения функции почек тяжелой степени тяжести (КК менее 30 мл/мин).
• Беременность и период кормления грудью.
Детский возраст (эффективность и безопасность не установлены).
С осторожностью
С осторожностью применять препарат у пациентов с нарушением функции почек легкой и средней степени тяжести (КК > 30 мл/мин). Следует соблюдать осторожность при одновременном применении с другими препаратами, способными вызывать гипокальциемию (например, аминогликозиды, кальцитонин, «петлевые» диуретики) в связи с риском развития синергического эффекта, приводящего к гипокальциемии тяжелой степени тяжести. С осторожностью следует применять препарат одновременно с другими препаратами, обладающими нефротоксичным потенциалом. С осторожностью следует применять одновременно с антиангиогенными препаратами в связи с увеличением риска развития остеонекроза челюсти. Соблюдать осторожность при применении у пациентов с нарушением функции печени тяжелой степени тяжести в связи с ограниченностью данных по применению препарата у пациентов данной категории.
Применение при беременности и в период грудного вскармливания
Применение препарата Золедроновая кислота во время беременности противопоказано.
Препарат Золедроновая кислота может оказывать неблагоприятное воздействие на плод. В исследованиях у животных выявлено токсическое воздействие на репродуктивную функцию. Нет данных о применении препарата во время беременности у человека.
При возникновении беременности во время терапии бифосфонатами возможен риск возникновения внутриутробных пороков развития плода (например, аномалий развития скелета и других аномалий). Зависимость риска от величины временного промежутка между прекращением терапии бифосфонатами и моментом зачатия, пути введения и особенностей конкретного препарата неизвестна.
Женщины репродуктивного возраста должны быть предупреждены о необходимости применять надежные методы контрацепции во время лечения препаратом Золедроновая кислота.
Неизвестно, проникает ли золедроновая кислота в грудное молоко. Применение препарата Золедроновая кислота в период грудного вскармливания противопоказано.
В исследованиях у животных золедроновая кислота подавляла фертильность в дозе 0,1 мг/кг в сутки. Нет данных о влиянии золедроновой кислоты на фертильность у человека.
Способ применения и дозы
Метастазы в кости при злокачественных солидных опухолях и множественной миеломе:
Взрослые и пациенты пожилого возраста
Рекомендуемая доза составляет 4 мг внутривенно капельно, в течение не менее 15 мин каждые 3-4 недели. Перед введением препарата разводят концентрат (содержимое 1 флакона) 100 мл раствора для инфузий, не содержащего кальций (0,9 % раствор натрия хлорида или 5 % раствора декстрозы).
Пациентам также следует дополнительно назначать кальций внутрь в дозе 500 мг в сутки и витамин D внутрь в дозе 400 МЕ в сутки.
Гиперкальциемия, обусловленная злокачественными опухолями:
Взрослые и пациенты пожилого возраста
При гиперкальциемии (концентрация скорректированного по альбумину сывороточного кальция ? 12 мг/дл или 3 ммоль/л) рекомендуемая однократно вводимая доза препарата составляет 4 мг. Для обеспечения адекватности гидратации пациента рекомендуется введение физиологического раствора перед, одновременно или после инфузии золедроновой кислоты.
Пациенты с нарушением функции почек
Гиперкальциемия, обусловленная злокачественными опухолями:
Решение о лечении золедроновой кислотой пациентов с выраженными нарушениями функции почек следует принимать только после тщательной оценки риска применения препарата и ожидаемой пользы терапии. Пациентам, у которых концентрация креатинина в сыворотки крови составляет < 400 мкмоль/л или < 4,5 мг/дл, не требуется коррекция режима дозирования.
Костные метастазы распространенных злокачественных опухолей и множественная миелома:
Доза золедроновой кислоты зависит от исходного уровня клиренса креатинина, рассчитанного по формуле Cockcroft-Gault. Не рекомендуется принимать золедроновую кислоту у пациентов с тяжелыми нарушениями функции почек (значения клиренса креатинина < 30 мл/мин).
Рекомендуемые дозы у пациентов с легкими или умеренными нарушениями функции почек (значения клиренса креатинина 30-60 мл/мин) приведены ниже.
Исходное значение клиренса креатинина (мл/мин) Рекомендуемая доза Золедроновой
кислоты
> 60
50-60
40-49
30-39 4.0 мг (5 мл концентрата)
3,5 мг (4,4 мл концентрата)
3,3 мг (4,1 мл концентрата)
3,0 мг (3,8 мл концентрата)
После начала терапии следует проводить определение концентрации сывороточного креатинина перед введением каждой дозы препарата. При выявлении нарушений функции почек очередное введение золедроновой кислоты следует отложить. Нарушения функции почек определяются по следующим параметрам:
• Для пациентов с нормальной исходной концентрацией креатинина в сыворотке крови (< 1,4 мг/дл) – повышение концентрации креатинина на 0,5 мг/дл
• Для пациентов с измененной исходной концентрацией креатинина в сыворотке крови (> 1,4 мг/дл) – повышение концентрации креатинина на 1 мг/дл.
Терапию золедроновой кислотой возобновляют только после того, как уровень креатинина достигает значений в пределах ± 10 % от исходной величины, в той же дозе, которая применялась до прерывания лечения.
Приготовление раствора для инфузий
Из концентрата 4 мг/5 мл (содержимое 1 флакона) готовят раствор для инфузий в асептических условиях. Перед введением препарата разводят концентрат (содержимое 1 флакона или меньший объем, если требуется) 100 мл раствора для инфузий, не содержащего кальций (0,9 % раствор натрия хлорида или 5 % раствор декстрозы).
Приготовленный раствор золедроновой кислоты желательно использовать непосредственно после приготовления. Неиспользованный сразу раствор можно хранить в асептических условиях в холодильнике при температуре +2-8°С не более 24 часов. Перед введением раствор следует выдержать в помещении до достижения им комнатной температуры.
Общее время между разведением концентрата, хранением приготовленного раствора в асептических условиях в холодильнике при температуре +2-8°С и окончанием введения препарата не должно превышать 24 часа.
Раствор золедроновой кислоты не следует смешивать с любыми другими лекарственными препаратами. Препарат не следует смешивать с какими-либо растворами, содержащими кальций и любые другие двухвалентные катионы, такими как раствор Рингера. Для введения раствора золедроновой кислоты всегда следует использовать отдельную систему для инфузий.
Побочное действие
Нежелательные реакции перечислены ниже по органам и системам с указанием частоты их возникновения. Критерии частоты: очень часто (>=1/10), часто (?1/100, <1/10), иногда (>=1/1000, <1/100), редко (>=1/10000, <1/1,000), очень редко (<1/10000), включая отдельные сообщения.
Нарушения со стороны крови и лимфатической системы: часто – анемия, иногда – тромбоцитопения, лейкопения; редко – панцитопения.
Нарушения со стороны нервной системы: часто – головная боль, парестезии; нечасто – головокружение, дисгевзия, гипестезия, гиперестезия, тремор; очень редко – судороги, кинестезия и тетания (развивающиеся вследствие гипокальциемии).
Нарушения психики: часто – нарушение сна; нечасто – чувство тревоги; редко – спутанность сознания.
Нарушения со стороны органа зрения: часто – конъюнктивит; иногда – «размытость» зрения; очень редко – увеит, эписклерит.
Нарушения со стороны желудочно-кишечного тракта: часто – тошнота, рвота, анорексия; иногда – диарея, запор, абдоминальные боли, диспепсия, стоматит, сухость во рту.
Нарушения со стороны дыхательной системы, органов грудной клетки и средостения: иногда – отдышка, кашель; редко – интерстициальная болезнь легких.
Нарушения со стороны кожи и подкожных тканей: иногда – зуд, сыпь (включая эритематозную и макулярную), повышенная потливость.
Нарушения со стороны костно-мышечной и соединительной ткани: часто – боль в костях, миалгия, артралгия, генерализованные боли, тугоподвижность суставов; нечасто – некроз челюсти, мышечные судороги.
Нарушения со стороны сердца и сосудов: иногда – выраженное повышение или снижение артериального давления; редко – брадикардия; аритмия (развивающаяся вследствие гипокальциемии).
Нарушения со стороны почек и мочевыводящих путей: часто – нарушения функции почек; иногда – острая почечная недостаточность, гематурия, протеинурия.
Нарушения со стороны иммунной системы: иногда – реакции повышенной чувствительности; редко – ангионевротический отек.
Лабораторные и инструментальные данные: очень часто – гипофосфатемия; часто – повышение сывороточных концентраций креатинина и мочевины, гипокальциемия; иногда – гипомагниемия, гипокалиемия; редко – гиперкалиемия, гипернатриемия.
Общие расстройства и нарушения в месте введения: часто – реакция острой фазы, повышение температуры тела, гриппоподобный синдром (включающее общее недомогание, озноб, чувство недомогания, «приливы»), периферические отеки, астения; нечасто – реакции в месте введения (боль, раздражение, отечность, уплотнение, покраснение), боль в грудной клетке, увеличение массы тела; редко – артрит и опухание суставов как симптом реакции острой фазы.
Следует иметь в виду, что при применении других бисфосфонатов у пациентов с бронхиальной астмой, чувствительных к ацетилсалициловой кислоте, отмечались случаи бронхоспазма, однако при применении золедроновой кислоты данного явления не наблюдалось.
При лечении пациентов бисфосфонатами в клинической практике описаны редкие случаи развития остеонекроза челюсти (обычно после экстракции зуба или другого стоматологического вмешательства). Четкая причинная связь развития остеонекроза не установлена.
Нежелательные явления по данным спонтанных отчетов и литературных сообщений (частота неизвестна).
Нарушения со стороны иммунной системы: анафилактическая реакция/шок.
Нарушения со стороны нервной системы: сонливость.
Нарушения со стороны органа зрения: эписклерит, склерит и воспалительные заболевания орбиты.
Нарушения со стороны сердца: фибрилляция предсердий.
Нарушения со стороны сосудов: снижение артериального давления, приводящее к обмороку или циркуляторному коллапсу, в основном, у пациентов с факторами риска.
Нарушения со стороны дыхательной системы, органов грудной клетки и средостения: бронхоспазм.
Нарушения со стороны кожи и подкожных тканей: крапивница.
Нарушения со стороны скелетно-мышечной и соединительной ткани: внезапное выраженное ограничение подвижности суставов и/или тяжелая и в некоторых случаях ограничивающая трудоспособность боль в костях, суставах и/или мышцах, атипичные подвертельные и диафизарные переломы бедренной кости.
Передозировка
При острой передозировке препарата (ограниченные данные) отмечались нарушения функции почек, включая почечную недостаточность, изменения электролитного состава, включая концентрацию кальция, фосфатов и магния в плазме крови. Пациент, получивший дозу препарата, превышающую рекомендованную, должен находиться под постоянным наблюдением. В случае возникновения гипокальциемии, сопровождающейся клиническими проявлениями, показано проведение инфузии кальция глюконата.
Взаимодействие с другими лекарственными средствами
При одновременном применении с золедроновой кислотой других часто применяемых лекарственных препаратов (противоопухолевые средства, диуретики, антибиотики, анальгетики) каких-либо клинически значимых взаимодействий не отмечено.
По данным, полученным в исследованиях in vitro, золедроновая кислота не имеет существенного связывания с белками плазмы и не ингибирует изоферменты системы цитохрома Р450. Тем не менее, специальные клинические исследования по изучению лекарственного взаимодействия не проводились. Рекомендуется соблюдать осторожность при одновременном применении бисфосфонатов с аминогликозидами, кальцитонином, «петлевыми» диуретиками, поскольку одновременное назначение этих препаратов обуславливает более продолжительное снижение концентрации кальция в плазме крови.
Необходима осторожность при одновременном применении Золедроновой кислоты с препаратами, потенциально обладающими нефротоксическим действием. Следует также иметь в виду вероятность развития гипомагниемии. У пациентов с множественной миеломой возможно повышение риска развития нарушений функции почек при внутривенном введении бисфосфонатов, таких как золедроновая кислота, в комбинации с талидомидом.
Фармацевтическое взаимодействие и вопросы совместимости
Разведенный раствор золедроновой кислоты нельзя смешивать с инфузионными растворами, содержащими ионы кальция, например, раствором Рингера.
При использовании для введения золедроновой кислоты стеклянных флаконов, инфузионных систем и мешков разных типов, изготовленных из поливинилхлорида, полиэтилена и полипропилена (предварительно заполненных 0,9 % раствором натрия хлорида или 5 % раствором декстрозы) каких-либо признаков несовместимости с золедроновой кислотой не обнаружено.
Особые указания
Перед инфузией следует убедиться в адекватности гидротации у пациента. При необходимости рекомендуется введение 0,9 % раствора натрия хлорида перед, параллельно или после инфузии золедроновой кислоты. Следует избегать гипергидрадации пациента из-за риска возникновения осложнений со стороны сердечно-сосудистой системы.
После введения золедроновой кислоты необходим постоянный контроль за концентрацией кальция, фосфора, магния и креатинина в сыворотке крови. При развитии гипокальциемии, гипофосфатемии или гипомагниемии может возникнуть необходимость в кратковременном дополнительном введении соответствующих веществ. У пациентов с нелеченной гиперкальциемией как правило имеется нарушение функции почек, поэтому необходим тщательный мониторинг функции почек у данной категории больных.
При решении вопроса о лечении золедроновой кислотой пациентов с костными метастазами с целью снижения риска патологических переломов, компрессии спинного мозга, гиперкальциемии, обусловленной опухолью, и снижения потребности в проведении лучевой терапии или оперативных вмешательств на кости, следует принимать во внимание, что терапевтический эффект наступает через 2-3 месяца после начала лечения золедроновой кислотой.
Нарушение функции почек
Имеются отдельные сообщения о нарушении функции почек на фоне применения бисфосфонатов. К факторам риска возникновения подобных осложнений относятся дигидратация, предшествующая почечная недостаточность, многократное введение Золедроновой кислоты или других бисфосфонатов, а также применение нефротоксичных лекарственных средств, и слишком быстрое введение препарата. Несмотря на то, что риск вышеописанных осложнений снижается при условии введения золедроновой кислоты в дозе 4 мг в течении не менее 15 минут, возможность нарушения функции почек сохраняется. Отмечались случаи нарушения функции почек, прогрессирования почечной недостаточности и возникновения необходимости в проведении гемодиализа при первом или однократном применении препарата.
Повышение сывороточной концентрации креатинина также наблюдается у некоторых пациентов при длительном применении Золедроновой кислоты в рекомендуемых дозах, хотя менее часто.
Поскольку имеются ограничения клинические данные по применению препарата у пациентов с тяжелой печеночной недостаточностью, не представляется возможным дать специфические рекомендации для данной категории пациентов.
Остеонекроз
Описаны случаи остеонекроза челюсти, в основном у пациентов с онкологическими заболеваниями на фоне лечения бисфосфонатами, в том числе золедроновой кислотой. Многие из таких пациентов получали одновременную терапию глюкокортикостероидами или химиотерапию. У многих пациентов имели место признаки местного инфекционно-воспалительного процесса, включая остеомиелит.
В клинической практике наиболее часто развитие остеонекроза челюсти отмечалось у пациентов с распрстраненным раком молочной железы и миеломной болезнью, а также при наличии стоматологических заболеваний (после удаления зуба, при заболеваниях пародонта, неудовлетворительной фиксации зубных протезов). Известными факторами риска остеонекроза челюсти являются рак, одновременная терапия (химиотерапия, лучевая терапия, антиангиогенные препараты, глюкокортикостероиды), сопутствующие состояния (анемия, коагулопатии, инфекция, предшествующее заболевание полости рта).
Перед применением бисфосфонатов у пациентов с онкологическими заболеваниями следует провести стоматологическое обследование и выполнить необходимые профилактические процедуры, а также рекомендовать строгое соблюдение гигиены полости рта.
Во время лечения бисфосфонатами следует по возможности избегать стоматологических инвазивных вмешательств. У пациентов с остеонекрозом челюсти, возникшем на фоне терапии бисфосфонатами, проведение инвазивного стоматологического вмешательства может способствовать ухудшению состояния. Нет данных, что прерывание лечения бисфосфонатами перед проведением стоматологического вмешательства снижает риск остеонекроза челюсти. План лечения конкретного пациента должен основываться на индивидуальной оценке соотношения риск/польза.
Описаны случаи остеонекроза иной локализации, в т.ч., тазовой кости, бедренной кости, наружного слухового канала, в основном у взрослых пациентов с онкологическими заболеваниями, получающих терапию бисфосфонатами, в т.ч. золедроновой кислотой.
Атипичные переломы бедренной кости
Описаны случаи возникновения атипичных подвертельных и диафизарных переломов бедренной кости у пациентов, длительное время получающих лечение бисфосфонатами по поводу остеопороза. Поперечные или короткие косые переломы могут локализоваться в любом месте на протяжении бедренной кости от малого вертела до надмыщелковой ямки. Описанные переломы возникают после минимальной травмы или самопроизвольно. Некоторые пациенты испытывают боли в бедре или в паху, часто сопровождающиеся признаками стрессовых переломов по результатам визуализирующих диагностических исследований, которые возникают за недели и месяцы до развития полного (завершенного) перелома бедренной кости. Нередко переломы возникают с обеих сторон, поэтому при возникновении перелома бедренной кости у пациента, получающего терапию бисфосфонатами, следует провести обследование контрлатеральной бедренной кости. Сообщалось также о медленном заживлении (срастании) этих переломов. Были получены сообщения об атипичных переломах бедренной кости у пациентов, получавших лечение золедроновой кислотой, однако причинно-следственная связь этих переломов с терапией золедроновой кислотой не была установлена. Решение о прекращении терапии препаратом у пациентов с подозрением на атипичный перелом бедренной кости до проведения обследования должно основываться на индивидуальной оценке соотношения ожидаемой пользы к возможному риску.
Пациентов, получающих терапию препаратом Золедроновая кислота, следует предупредить о необходимости сообщать медицинскому персоналу о любых болях в бедре или паховой области; каждый пациент, предъявляющий жалобы на такие симптомы, должен быть обследован до выявления возможного незавершенного (неполного) перелома бедренной кости.
Мышечная боль
В клинической практике сообщалось о нечастых случаях развития сильной и в некоторых случаях ограничивающей трудоспособность боли в костях, суставах и мышцах на фоне лечения бисфосфонатами, к которым относится и золедроновая кислота. Указанные симптомы развивались в течение периода от одного дня до нескольких месяцев после начала лечения. После прекращения лечения у большинства пациентов отмечено разрешение симптомов. У нескольких пациентов симптомы повторялись при возобновлении терапии или применении другого бисфосфоната.
Гипокальциемия
В клинической практике сообщалось о развитии гипокальциемии у пациентов, получающих лечение золедроновой кислотой. В случае развития тяжелой гипокальциемии отмечалось развитие нежелательных явлений со стороны нервной системы (судороги, тетания и онемение), сердечной аритмии. В некоторых случаях гипокальциемия может представлять угрозу для жизни.
Следует соблюдать осторожность при прменении препарата Золедроновая кислота одновременно с другими лекарственными средствами, способными вызвать гипокальциемию, поскольку это может привести к синергическому взаимодействию и развитию гипокальциемии тяжелой степени. Перед началом терапии препаратом Золедроновая кислота следует определить уровень кальция в сыворотке и скорректировать гипокальциемию. Пациенты должны получать адекватное восполнение препаратами кальция и витамин D.
Пациенты, получающие терапию препаратом Золедроновая кислота, не должны одновременно получать препарат Акласта, так же как и другие бисфосфонаты.
Эффективность и безопасность применения препарата Золедроновая кислота в педиатрической практике до настоящего времени не установлены.
Влияние на способность к вождению транспортных средств и работу с машинами и
механизмами
Данные о влиянии золедроновой кислоты на способность к вождению транспортных средств отсутствуют. Однако следует помнить о возможном возникновении головокружения и спутанности сознания при терапии золедроновой кислотой.
Форма выпуска
Концентрат для приготовления раствора для инфузий 4 мг/5 мл. По 5 мл препарата в бесцветный пластиковый флакон, укупоренный резиновой пробкой, обкатанной алюминиевым колпачком с пластиковой отщелкивающейся крышкой. По 1 флакону вместе с инструкцией по применению в пачку картонную.
Условия хранения
В защищенном от света месте при температуре не выше 25°С. Хранить в недоступном для детей месте.
Срок годности
3 года. Препарат не следует использовать по истечении срока годности, указанного на упаковке.
Условия отпуска из аптек
Отпускают по рецепту.
Наименование держателя или владельца регистрационного удостоверения лекарственного препарата
ООО "Мир-Фарм", Россия
Регистрационное удостоверение ЛП-003688 от 20.06.2016 г. Дата переоформления 21.06.2021. Дата окончания действия 31.12.2025
№ п/п Стадия производства Производитель Адрес производителя Страна
1 Упаковщик/фасовщик (вторичная/третичная упаковка) Закрытое акционерное общество "Обнинская химико-фармацевтическая компания" (ЗАО "ОХФК") Калужская область, г. Обнинск, Киевское шоссе, зд. 107 Россия
2 Упаковщик/фасовщик (вторичная/третичная упаковка) Фармидея ООО Rupnicu iela 4, Olaines, Olaines novads, LV-2114, Latvia Латвия
3 Упаковщик/фасовщик (в первичную упаковку) Фармидея ООО Rupnicu iela 4, Olaines, Olaines novads, LV-2114, Latvia Латвия
4 Производитель (готовой ЛФ) Фармидея ООО Rupnicu iela 4, Olaines, Olaines novads, LV-2114, Latvia Латвия
5 Выпускающий контроль качества Закрытое акционерное общество "Обнинская химико-фармацевтическая компания" (ЗАО "ОХФК") Калужская область, г.о. "Город Обнинск", г. Обнинск, Киевское шоссе, зд. 3а, стр. 3 Россия
6 Выпускающий контроль качества Фармидея ООО Rupnicu iela 4, Olaines, Olaines novads, LV-2114, Latvia Латвия